蚊媒传染病,是由病媒蚊子传播的危害性较强的传染病。蚊媒病毒(如基孔肯雅热、寨卡病毒、登革病毒、黄热病毒等)已对全球公共卫生构成重大威胁,但传统诊断方法存在灵敏度不足、污染风险高、依赖专业实验室等局限。
深圳大学化学与环境工程学院刘翼振副教授与深圳市第二人民医院顾大勇主任医师合作,报道了一种新型通用光控CRISPR/Cas12a超敏检测技术,通过工程化crRNA 3’末端修饰实现蚊媒病毒的一锅法高效检测。相关成果以“A universal Cas12a activity regulation strategy via photocleavable crRNA 3’-terminal additives enables one-pot CRISPR detection of arboviruses”为题发表在国际权威期刊Chemical Engineering Journal上(影响因子13.2,DOI: https://doi.org/10.1016/j.cej.2025.166699)。副研究员庄松宽、2022级化学(师范)本科生董粤瑜为共同第一作者,顾大勇主任医师和刘翼振副教授为共同通讯作者,深圳大学为第一完成单位。
本研究开发了一种通用光控CRISPR/Cas12a一锅法检测平台,通过在crRNA 3’末端引入光可切割(PC)DNA linker修饰,实现了虫媒病毒的快速、高灵敏度检测,整个流程可在30分钟内完成。 临床样本检测结果证实,该平台对12份虫媒病毒样本(6份黄热病毒阳性、6份阴性对照)的检测结果与RT-qPCR 100%吻合,且能精准区分黄热病毒与寨卡、登革等其他蚊媒病毒。
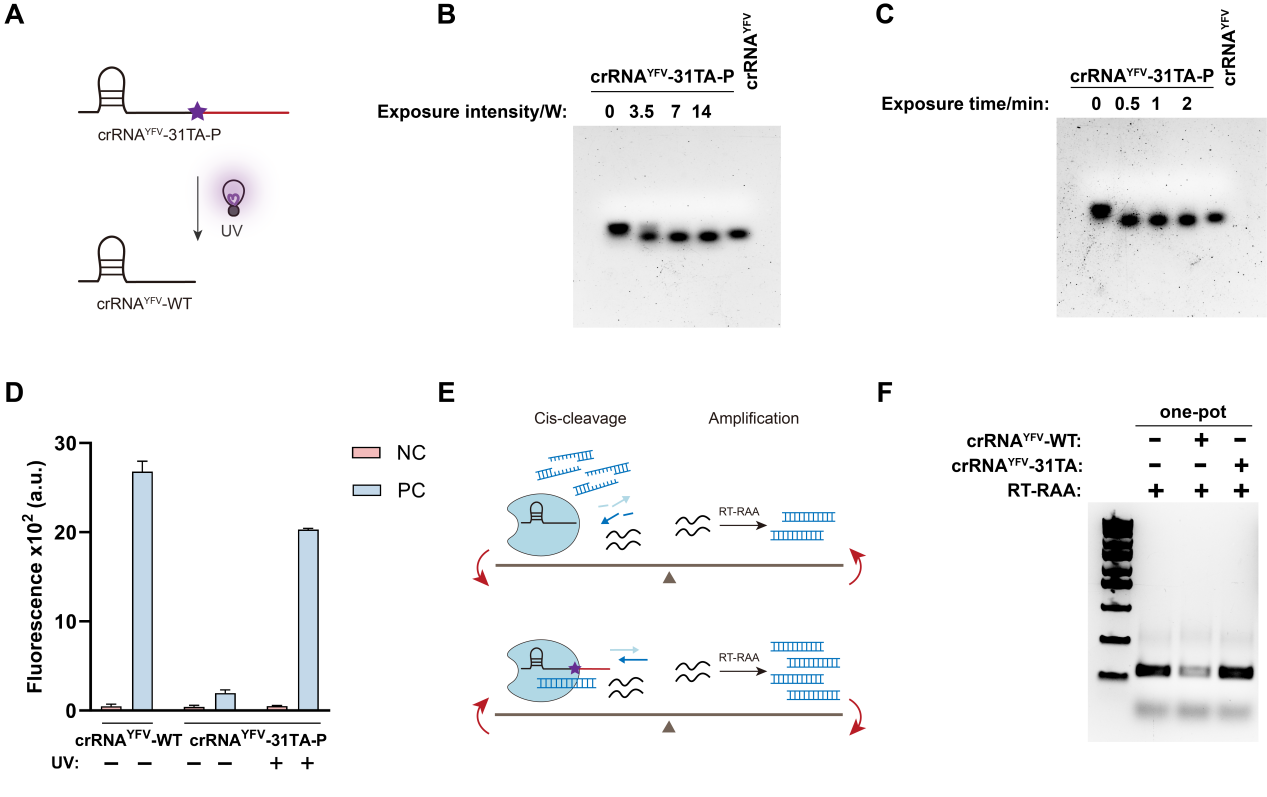
该研究建立的通用光控CRISPR/Cas12a平台实现单管内逆转录重组酶扩增(RT-RAA)与CRISPR检测的时序整合,在37-42℃恒温条件下完成检测。其核心创新在于利用crRNA 3’末端修饰诱导Cas12a/crRNA-DNA三元复合物构象扭曲,实现对Cas12a活性的广谱抑制;结合光可切割linker,经UV照射(14 W,0.5 min)即可解除抑制,无需靶标特异性优化。该平台展现出1 aM(0.6 copies/μL)的超高灵敏度,解决了传统CRISPR检测中扩增与检测竞争、需反复优化的问题,为蚊媒病毒的床旁快速诊断及疫情应急响应提供了高效工具。
本研究得到了国家重点研发计划项目、深圳市医学研究专项资金项目、广东省基础与应用基础研究基金以及深圳市科技计划项目的支持。
